A legjobb adjuváns a tüdőrák kemoterápiájához. | 1 + 1> 487%
tüdőrák / SCLC / NSCLC
Hatékonyan javítja a kemoterápiás hatást, a kezelést, az immunitást.
Csökkentse a mellékhatásokat és az ismétlődést.
Kombinált terápia | Áttekintés / Kapcsolat / Absztrakt / Szerep / Alapelv / Cselekvés / Mechanizmus / Funkció / Munka.
Absztrakt / összefoglalás / A tüdőrák áttekintése. (SCLC / NSCLC)
Mi az apoptózis?
Solamargine (szerep, elv, cselekvés, mechanizmus, funkció, munka)
A legjobb adjuváns a tüdőrák kemoterápiájához. (SCLC / NSCLC) | 1+1>487%
Hatékonyan javítja a kemoterápiás hatást, a kezelést és az immunitást.
Csökkentse a mellékhatásokat és az ismétlődést Kombinált terápia.
1. Az Solamargine hatása a TNF-ekre és a ciszplatin-rezisztens humán tüdőrákos sejtekre. (Solamargine hatása az emberi tüdőrákos sejtekre - a rákos sejtek TNF-ekre való hajlamának fokozása.)
2. A PI3-K / Akt inaktiválása, valamint az SP1 és p65 expresszió csökkentése növeli az Solamargine hatását az EP4 expressziójának elnyomására az emberi tüdőrákos sejtekben.
3. Az lncRNS HOTAIR és a miR-214-3p újszerű kölcsönös kölcsönhatása hozzájárul az Solamargine gátolt PDPK1 génexpresszióhoz emberi tüdőrákban.
4. Az EP4 megcélzása a c-Jun downstream szakaszán keresztül a DNMT1 ERK1 / 2-mediált csökkentésével új mechanizmust tár fel az Solamargine gátolt tüdőráksejtek növekedésében.
5. A Solanum incanum kivonat (SR-T100) melanoma sejt apoptózist indukál és gátolja a kialakult tüdőmetasztázisokat.
Kombinált terápia A tüdőrákos sejtek (SCLC / NSCLC) kutatási eredményei.
Absztrakt / összefoglalás / A tüdőrák áttekintése. (SCLC / NSCLC)
A tüdőrák a leggyakoribb rák és a rákos halálozás vezető oka világszerte.
A tüdőrák szövettani jellemzőinek megfelelően két csoportra osztható: kissejtes tüdőrák (SCLC) és nem kissejtes tüdőrák (NSCLC).
Közülük a tüdőrák több mint 80% -a nem kissejtes tüdőrák (NSCLC), adenokarcinóma a legelterjedtebb altípus.
Az NSCLC-t mind a magas incidencia, mind a letalitás jellemzi, az ötéves túlélési arány az esetek kevesebb mint 10% -át teszi ki.
Noha a betegség biológiai jellemzőinek megértése és a multidiszciplináris terápiás megközelítések, például az egyéni kemoterápia, a célzott terápiák, az immunmódszerek és a jobb szupportív ellátás megértése nemrégiben történt előrelépés, az eredmény előrehaladott betegségben szenvedők számára továbbra is szomorú.
Ezért sürgősen szükség van hatékonyabb alternatív kezelési stratégiák keresésére az elhanyagolható mellékhatásokkal járó terápiás hatékonyság erősítése érdekében.
A gyógynövényekből származó természetes fitokemikáliák jelentős elismerést nyertek a karcinogenezis szabályozásában, és újszerű megközelítésnek tekintik őket a rák megelőzésében és kezelésében.
Mi az apoptózis?
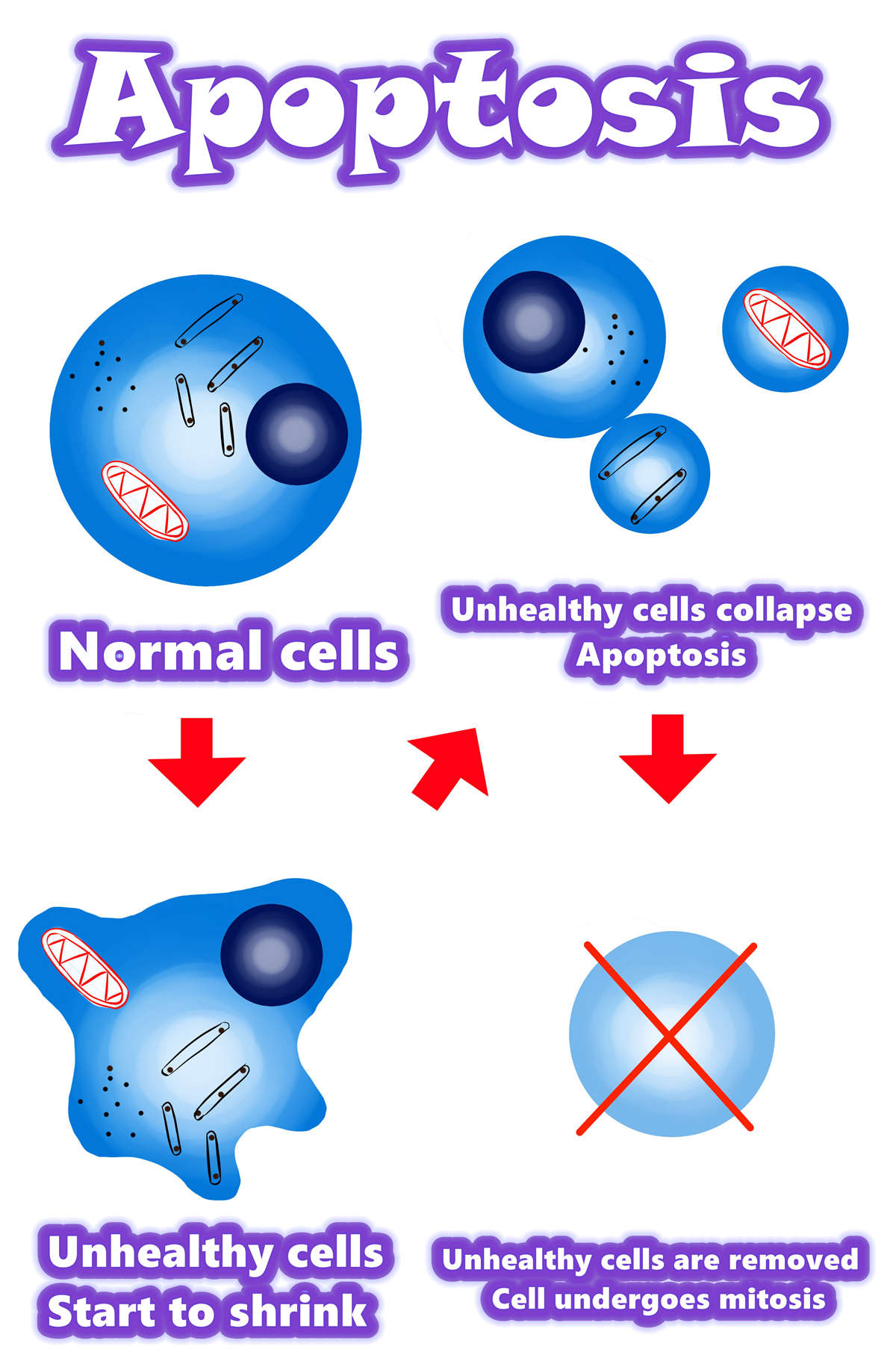
Az apoptózis áttekintése
• Programozott sejthalál.
• Az apoptózis a programozott sejthalál vagy a „sejtes öngyilkosság” egyik formája.
• Az apoptózis különbözik a nekrózistól, amelyben a sejtek elpusztulnak sérülés miatt.
• Az apoptózis eltávolítja a sejteket a fejlődés során, megszünteti a potenciálisan rákos és vírusfertőzött sejteket, és fenntartja az egyensúlyt a testben.
Miért mennek át a sejtek apoptózison?
Alapvetően az apoptózis egy általános és kényelmes módszer a sejtek eltávolítására, amelyek már nem lehetnek a szervezet részei.
Egyes sejtek rendellenesek, és életben maradva károsíthatják a szervezet többi részét, például vírusfertőzéssel vagy DNS károsodással rendelkező sejtek.
Az apoptózis a fejlődés része.
Sok organizmusban a programozott sejthalál a fejlődés normális része.
A rákos sejtek és az apoptózis kapcsolata.
Az apoptózis megszüntetheti a fertőzött vagy rákos sejteket.
Amikor egy sejt DNS-je megsérül, tipikusan észleli a kárt és megpróbálja helyrehozni.
Ha a károsodás helyrehozhatatlan, a sejt általában apoptózisba kerül, biztosítva, hogy a sérült DNS-t ne adja tovább.
Ha a sejteknek DNS-károsodásuk van, de nem mennek át apoptózison, akkor a rák felé vezető úton lehetnek.
A „sikeres” rákos sejtek azonban sikeresen kikerülik az apoptózis folyamatát.
Ez lehetővé teszi számukra az irányításon kívüli szétválást és a mutációk (DNS-ben bekövetkező változások) felhalmozódását.
Az apoptózis kulcsfontosságú az immunműködés szempontjából.
Az apoptózis szintén alapvető szerepet játszik az egészséges immunrendszer kialakulásában és fenntartásában.
Hol vannak a rákos sejtek gyengeségei és tünetei?
A rákos sejtek tünetei a magban vannak.
A mag szabályozza a külső citoplazmát, a sejtösszetételt, a sejt életképességét stb.
A DNS-mutációk a magban is mutálódnak.
Ezért a rákos sejtek kezeléséhez először be kell lépnünk a magba.
Hagyja, hogy a „szabályozó sejt gén” mechanizmusa belépjen a magba a szabályozáshoz.
Agresszívek a rákos sejtek?
Az Solamargine hatása után a rákos sejtek agresszivitása enyhül.
Tehát az Solamargine alkalmazása után sok beteg úgy érzi, hogy fele jobban vagyok.
Bár a daganat nem tűnik el gyorsan, a betegek úgy érzik, hogy az agresszivitás mértéke csökken.
Solamargine (szerep, elv, cselekvés, mechanizmus, funkció, munka)
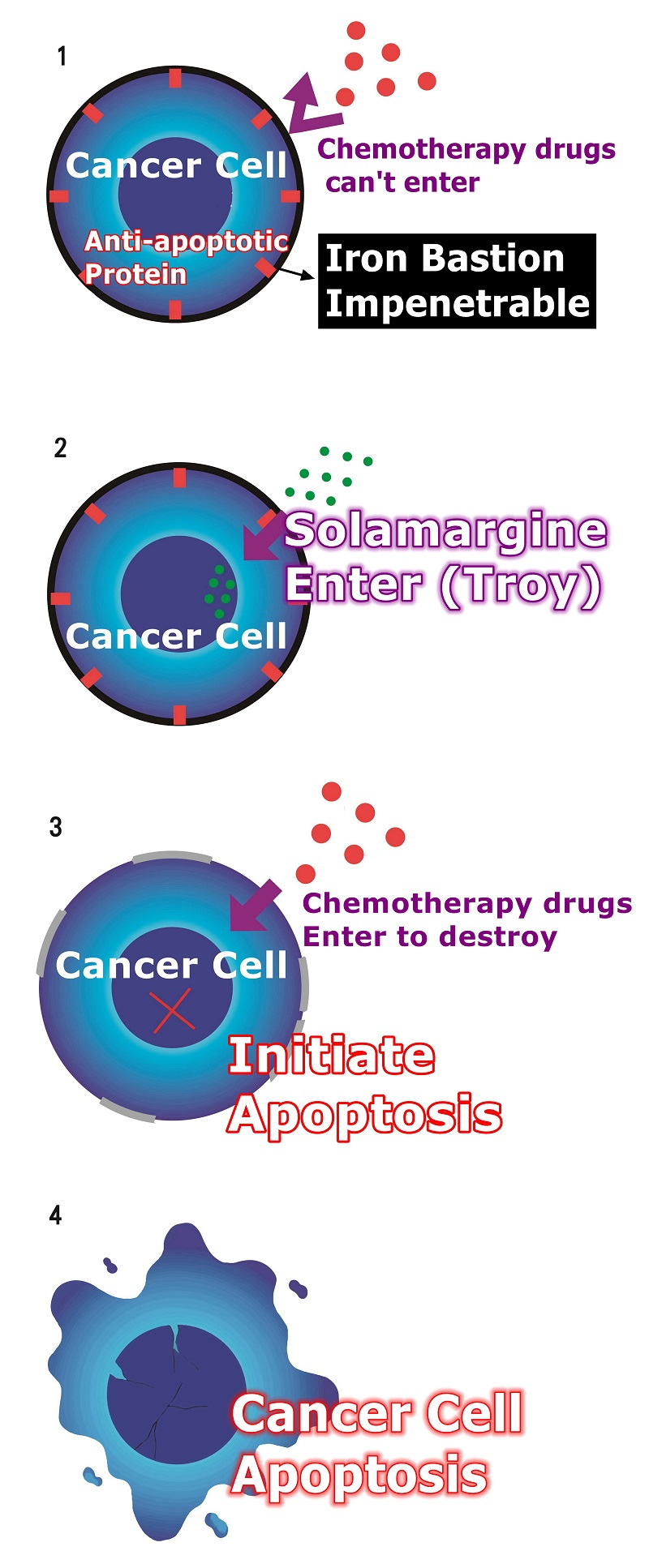
Az Solamargine fő funkciómechanizmusa, szerep, alapelv, cselekvés, mechanizmus, funkció, munka:
Amikor az Solamargine belép,
Az Solamargine aktiválja azokat a receptorokat, amelyeket a rákos sejtek kikapcsolnak, így a rákos sejtek újra modulálódhatnak.
Az Solamargine modulálja a rákos sejtek anti-moduláló génjeit, így a rákos sejtek kevésbé rezisztensek.
Csökkentett gyógyszerrezisztencia.
Amikor a rákos sejtek kevésbé rezisztensek a gyógyszerekkel szemben, a kemoterápia hatékonyabbá válik.
Az Solamargine modulálja a mutált géneket a rákos sejtekben, majd elindítja a rákos sejtek apoptózisát a rákellenes hatások elérése érdekében.
Az Solamargine mely kemoterápiás gyógyszerekkel kombinálva hatékonyabb a rákos sejtek kezelésében?
V: Ciszplatin, Áfonya, Metotrexát, 5-Fu.
A legjobb adjuváns a tüdőrák kemoterápiájához. | 1+1>487%
Hatékonyan javítja a kemoterápiás hatást, a kezelést, az immunitást.
Csökkentse a mellékhatásokat és az ismétlődést Kombinált terápia.
Áttekintés / Kapcsolat / Absztrakt / Szerep / Alapelv / Cselekvés / Mechanizmus / Funkció / Munka.
Solamargine vs rák
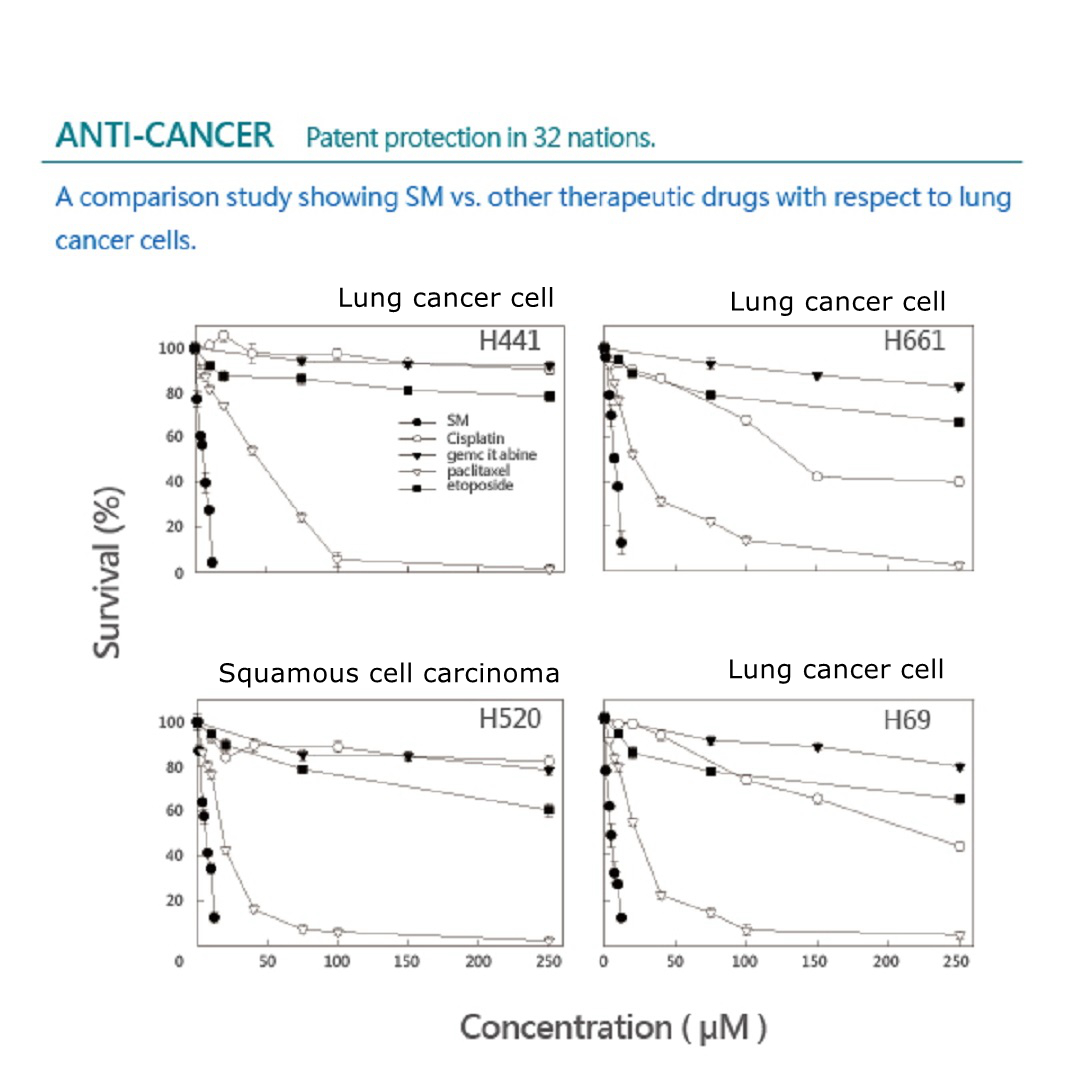
RÁK ELLENI
Szabadalmi oltalom 32 nemzetben.
Összehasonlító tanulmány, amely az Solamargine-t és más terápiás gyógyszereket mutatja a tüdőrákos sejtek tekintetében.
Az Solamargine, a hagyományos gyógynövényes gyógyszerből származó solanum lycocarpum gyümölcs glikoalkaloid kivonat tipikus metabolitjai nemcsak vírusellenes, gyulladáscsökkentő, hanem antiproliferatív aktivitást is kimutattak az emberi rák többféle típusa, beleértve a tüdőt is.
A Solanum incanum gyógynövényből izolált Solamargine négy citotoxicitást mutatott ki négy emberi tüdőrák sejtvonalban.
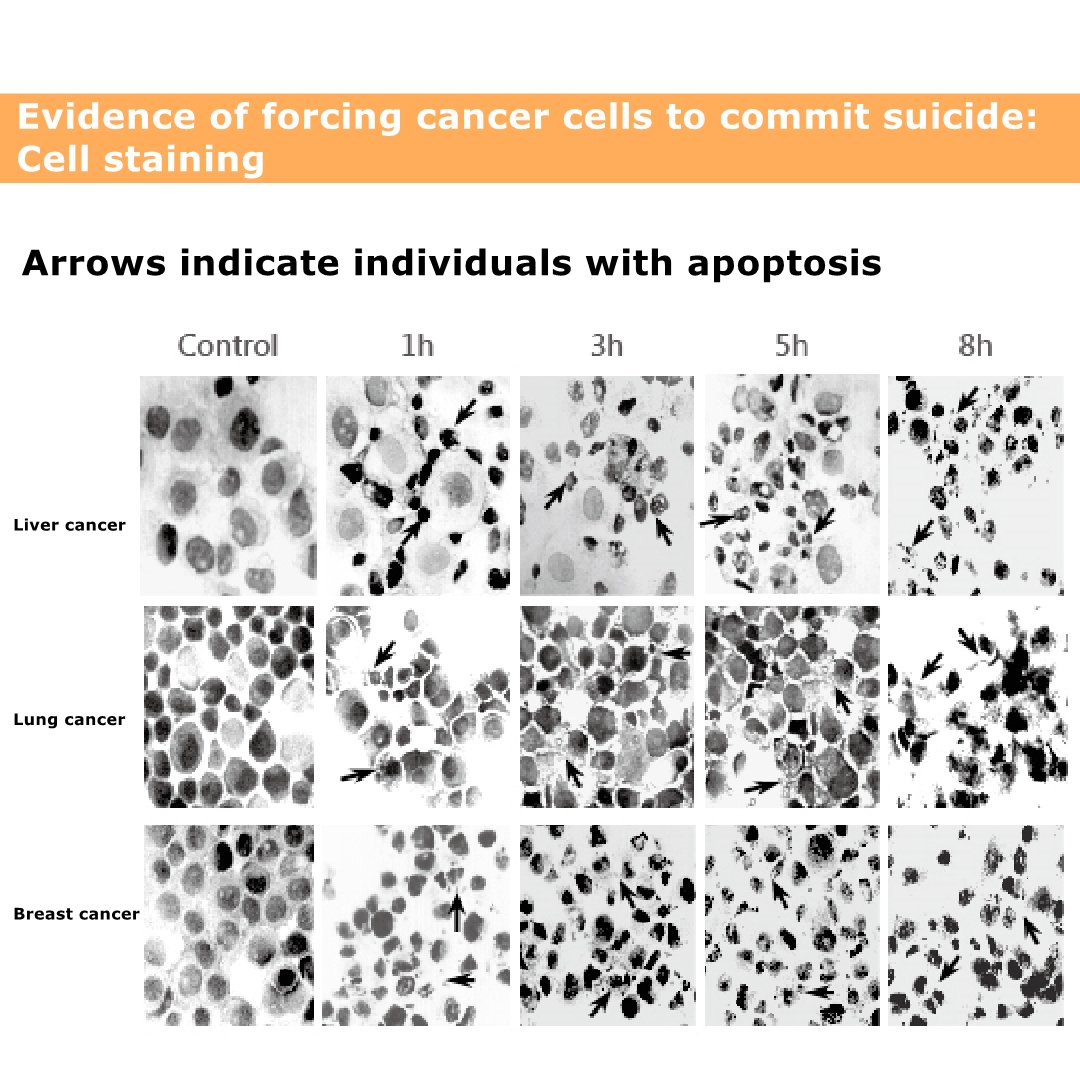
A kép rákos sejtek halálát mutatja.
A fekete és a fekete rész rákos sejtmag.
Még akkor is, ha a mag elszakad, a rákos sejtek elpusztulnak.
Az ábra azt mutatja, hogy a rákos sejtek halált okozhatnak.
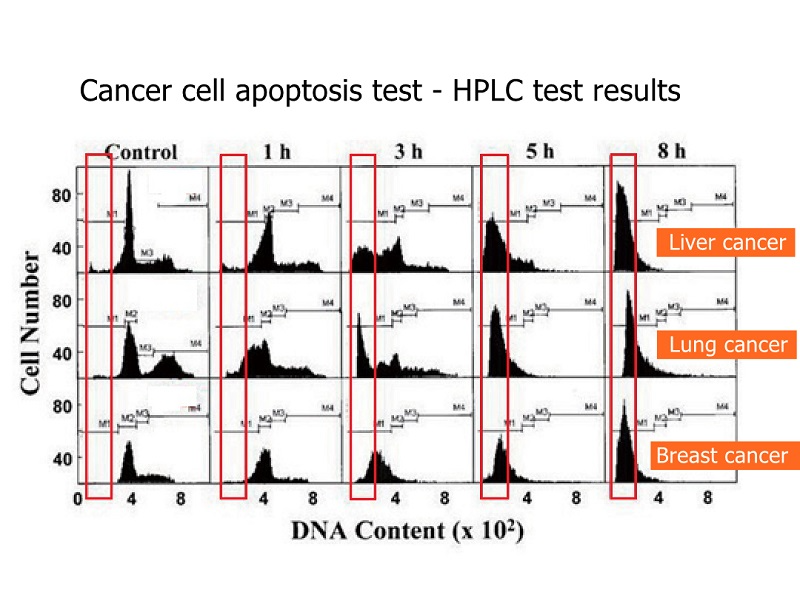
Az ábra azt mutatja, hogy a rákos sejtek halált okozhatnak.
Az ábra azt mutatja, hogy a tüdőrákos sejtek pusztulása viszonylag lassú, és csak nyolc óra múlva lesz nyilvánvaló.
Az ábra azt mutatja, hogy a májrákos sejtek halála nagyon nyilvánvaló, még nyilvánvalóbb nyolc óra alatt.
A grafikon azt mutatja, hogy az emlőrákos sejtek gyorsabban pusztulnak el. Már a kezdetektől nyilvánvaló volt, hogy az emlőrák kezelése könnyű, és az emlőrákban szenvedő betegeknek nem kell aggódniuk.
1. Az Solamargine hatása a TNF-ekre és a ciszplatin-rezisztens humán tüdőrákos sejtekre.
Az Solamargine hatása az emberi tüdőrákos sejtekre - a rákos sejtek TNF-ekre való hajlamának fokozása.
2. A PI3-K / Akt inaktiválása, valamint az SP1 és p65 expresszió csökkentése növeli az Solamargine hatását az EP4 expressziójának elnyomására az emberi tüdőrákos sejtekben.
3. Az lncRNS HOTAIR és a miR-214-3p újszerű kölcsönös kölcsönhatása hozzájárul az Solamargine gátolt PDPK1 génexpresszióhoz emberi tüdőrákban.
4. Az EP4 megcélzása a c-Jun downstream szakaszán keresztül a DNMT1 ERK1 / 2-mediált csökkentésével új mechanizmust tár fel az Solamargine gátolt tüdőráksejtek növekedésében.
5. A Solanum incanum kivonat (SR-T100) melanoma sejt apoptózist indukál és gátolja a kialakult tüdőáttétet.
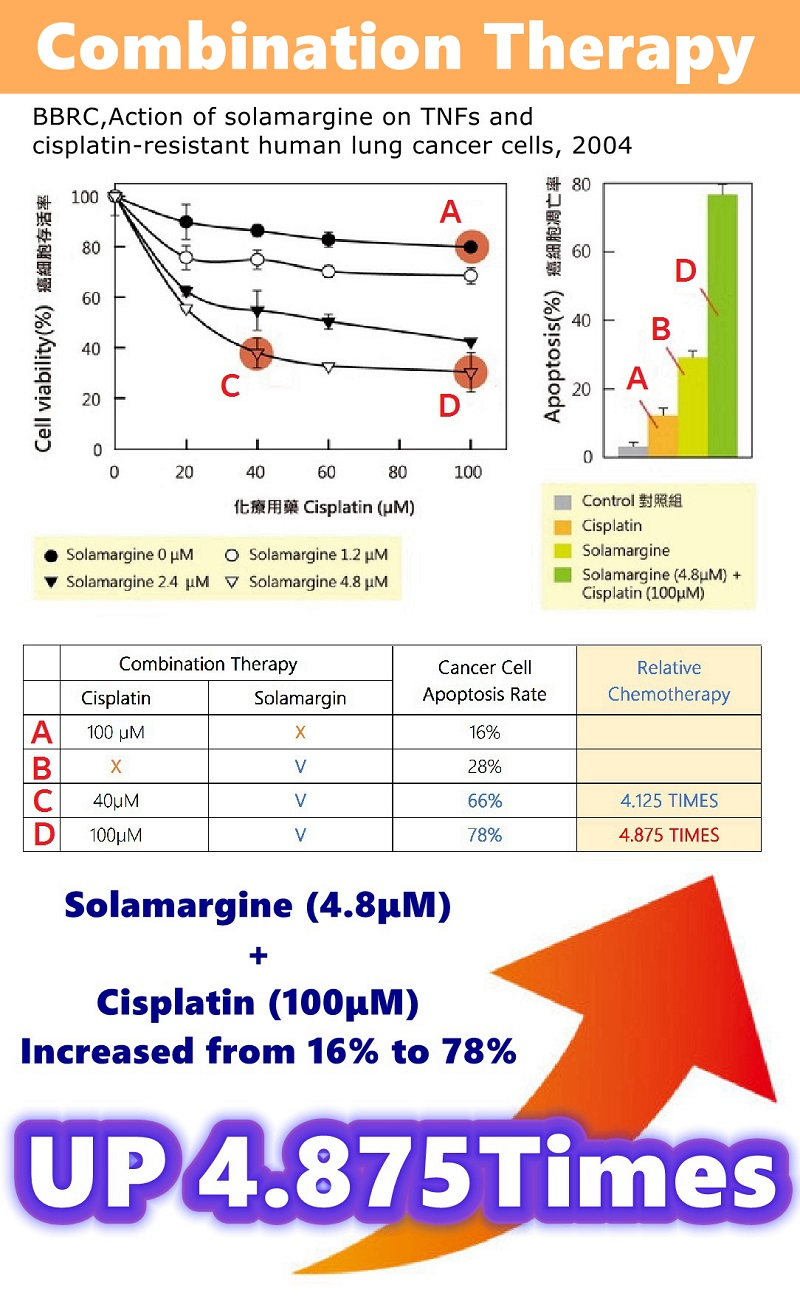
Kombinált terápia A tüdőrákos sejtek (SCLC / NSCLC) kutatási eredményei.
A. Ciszplatin (100 μM), a rákos sejtek apoptózisának 16% -a.
B. Egyedül SM (4,8 μM), a rákos sejtek apoptózisának 28% -a.
C. SM (4,80μM) + ciszplatin (40pμM), a rákos sejtek 66% -a apoptózis.
D. SM (4,80 μM) + ciszplatin (100 μM), a rákos sejtek apoptózisának 78% -a.
Az Solamargine tisztító hatása jobb, mint a ciszplatiné.
Az Solamargine és a Cisplatin együttes kezelése jelentősen növelte a tüdőrákos sejtek apoptózisát.
Az SM (4,8 μM) + a ciszplatin (40 μM) 16% -ról 66% -ra emelkedett (akár 4,255-szeresére).
Az SM (4,8 μM) + ciszplatin (100 μM), 16% -ról 78% -ra nőtt (akár 4,875-szeresére).
Átrendeződött: BBRC. Az Solamargine hatása a TNF-ekre és a gyógyszerrezisztens humán tüdőrákos sejtekre 2004
Az Solamargine hatása teljes mértékben kitöltötte az apoptózis kritériumait az emberi tüdőrákos sejtekben, és arra utalt, hogy az Solamargine apoptózissal okozta sejthalált.
Az Solamargine a sejt apoptózisát indukálja a TNFR-ek expressziójának és az azt követő TRADD / FADD-jelű kaszkádok modulálásával.
Az Solamargine a PDPK1 és a HOTAIR gátlásával, valamint a miR-214-3p jelátviteli tengely indukciójával gátolta az emberi tüdőrák sejtjeinek növekedését.
Az Solamargine az Akt inaktiválásával gátolja a tüdőrák sejtjeinek növekedését, majd az SP1 és a p65 csökkenését.
Az Solamargine gátolja a humán tüdőráksejtek növekedését a PGE2 receptor EP4 fehérje expressziójának csökkentése és az ERK1 / 2 jelátvitel indukálása révén.
Ezek az eredmények javítják az Solamargine rákellenes hatásában rejlő mechanizmusok megértését, és új molekuláris célpontokat nyújtanak az emberi tüdőrák kezelésében.